胶体的扩展
当我看到林耀宗写完了这篇理一下化学思路 - Liam’s boring life,并热情洋溢的让我审稿的时候,我很愉快的接下了这个任务。
接下来我提出了大量PR,但是都被驳回了,理由是太过超前。(〃>皿<)
因此我决定自己写一篇来继续深入探索胶体的种种性质。
前言
本文唯一的参考资料是一本破破烂烂的来源于二中图书馆的「无机化学」(武汉大学 吉林大学等校编)
此外,本文的目录结构保持与前文相同,以方便您的扩展阅读。作者突然想用FAQ的形式来写。
在您阅读本文前,我们已经假定您已经完全阅读并理解了理一下化学思路 - Liam’s boring life中的内容。
Q1:这个化学方程式算不算复分解反应?
$$ FeCl_{3} + 3H_{2}O == Fe(OH)_{3} +3HCl $$
这个化学式在初中没有讲过,我们暂且拓展一下。(盐类物质的水解属于高中范畴)
这里我们先假定了您已经知晓了电解质这一概念,并且明白水是极其微弱的电解质。
那么我们就可以将其看成一个离子反应,也就是说铁离子和水电离出来的氢氧根离子发生反应,进而生成氢氧化铁和氯化氢两种物质。
请注意这属于复分解反应的范畴,然而细心的同学可能就要问了:这里没有生成沉淀气体和水,不符合复分解反应的条件呀?
在这里我们将初中的课本进行一定的修正:
复分解反应发生的三个条件:
生成难溶性的物质
生成易挥发的物质
生成难电离的物质
这样子看来,氢氧化铁胶体就属于难溶性的物质,因此上述化学式属于复分解反应。
注:有些资料也把$HCl$归为易挥发的物质,在其后面加上箭头。
Q2:难溶性的氢氧化铁胶体为什么又处于介稳体系呢?
学过热力学的同学可能会对此产生疑问:胶体不是一个多相体系吗?其具有很大的界面,总有聚成更大粒子的倾向,当颗粒大到一定程度时,自然就会产生沉淀,也就是聚沉。但是为什么胶体不容易聚沉呢?
- 其一是因为它粒子较小,难以相遇。
- 其二是胶粒带相同电荷,相互排斥,不易聚沉。
- 其三是吸附层离子中的水化作用,使胶粒力被水包围。
Q3:电泳要用什么电?
因为胶粒带电荷,所以在电场作用下最外面的扩散层会和胶粒分开,向着电极移动,这就是电泳。
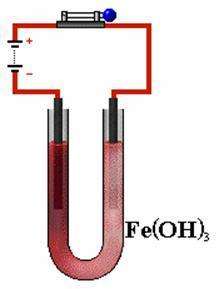
直流电,持续的电流才能有效破坏扩散层和吸附层之间的连接。
Q4:这些都是真正的胶体吗?

事实上稀豆浆、淀粉溶液并不属于胶体,严格意义上它们属于高分子溶液。
什么是高分子溶液?
橡胶,动物胶,蛋白质,淀粉等物质溶解于水或其他溶剂中,所得溶液叫做高分子溶液。
注意我们强调了「溶液」这一词,也就是说高分子溶液它是一个均相体系,在分散介质和分散相中不存在界面;而胶体则不同,胶体的胶粒和分散介质中有扩散层包裹着,属于一个多相体系。
之所以把它们归入胶体这一类,是因为它们的分子较大,具有某些胶体的性质,例如都可以产生丁达尔效应,都可以加入电解质而产生聚沉现象。
然而它们也有一定的不同之处,比如:(以下的胶体均指严格意义上的胶体)
- 胶体在聚成以后很难进行复原,而高分子溶液却很轻易的便可恢复成类胶体的性质。
- 高分的溶液和胶体的稳定性来源不同。高分子溶液之所以稳定,是因为它的高度溶剂化,不是由于电荷互相排斥(高分子溶液一般不带电荷)
Q5:不同的电解质对胶体的聚沉有影响吗?
有影响,其中关键影响如下:
- 只有与胶粒所带电荷电性相反的电解质粒子才起到关键的聚沉作用。(这个多好理解)
- 在相反的离子中粒子的种类与聚沉作用关系不大,决定电解质继承能力的离子的价态。
- 其中,价态越高,聚沉作用越强。
总结起来就是:
电解质的聚沉能力主要由异号的离子价态决定,离子价态越高,电解质的聚沉能力越大。
这一规律被称为叔儿采-哈迪规则。
Q6:高分子溶液对胶体的聚沉有影响吗?
当然有,而且还分两种影响。
保护作用
当向胶体中加入大量高分子溶液(即高分子数目远远超过胶体粒子的数目)完全覆盖其表面时,其对电解质聚沉的抵抗本领就会大为增强(也就是说同样数量的或者加入更多的电解质不能再引起胶体的聚沉)
实例:生活中的墨水就是一种常见的胶体,但我们几乎不会见到墨水聚沉,原因就在于墨水里面通常加入了阿拉伯胶或者明胶(更常用),由于高分子溶液是稳定的,也可以使得胶体获得稳定性。
敏化作用
与上述例子相反,单向胶体加入的高分子溶液不足以覆盖完胶体的表面时,它不仅不能对胶体产生保护作用,而且还会降低其稳定性,甚至引起聚沉。
由此可见,控制高分子溶液的用量对胶体的保护和敏化是非常重要的。
Q7:你能举一些有趣多样的胶体粒子吗?
这里列举两个能在高中阶段使用的物质制取的胶体:
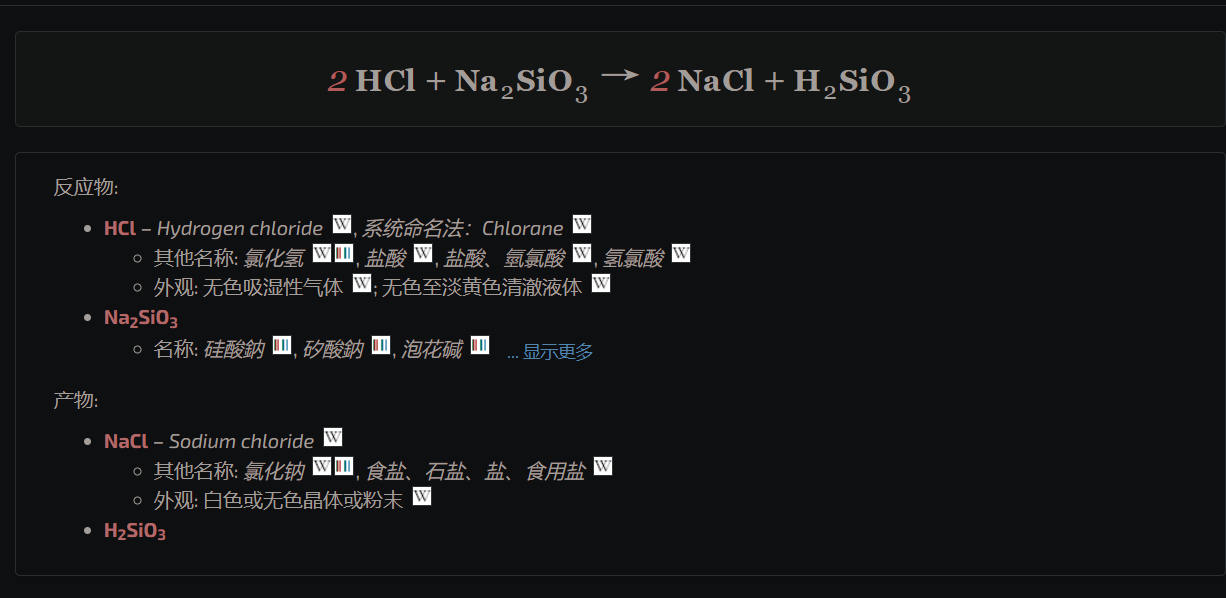

硫磺胶体的配平全是$1$。